معايرة الاحماض و القواعد
أمثلة على الأحماض.
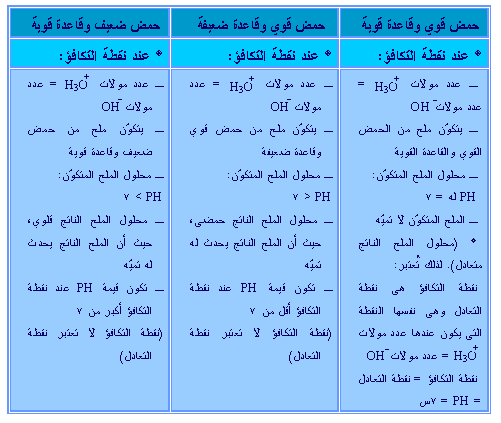
معايرة الاحماض و القواعد. Bases في القرن السابع عشر وأطلق على القواعد اسم القلويات وقد صن فها. أمثلة على القواعد. ـ تكون قيمة ph عند نقطة التكافؤ 7. تسمى تلك الطريقة طريقة جاي لو ساك وأحيانا تعزز رؤية نقطة اكتمال التفاعل عن طريق.
تستخدم فيها تفاعلات ترسيب. ي ظهر تفاعل أيونات الفضة ag مع أيونات الكلور cl ترسيب أبيض اللون عند نقطة اكتمال التفاعل. Robert boyle أول من قام بتصنيف المواد إلى أحماض بالإنجليزية. خصائص القواعد الأحماض والقواعد الأحماض والقواعد من أشهر الم رك بات الكيميائي ة.
الاحماض و القواعد المرافقة الحمض المرافق. الحموض و القواعد. 3 ـ معايرة حمض hcn مع naoh. و تتفاعل الأحماض مع أملاح الكربونات والكربونات الهيدروجينية وينتج ملح الحمض وماء وغاز ثاني أكسيد الكربون.
ي عد عالم الكيمياء روبرت بويل بالإنجليزية. هـ تتفاعل الأحماض مع القواعد وينتج ملح الحمض والماء غالبا.